
▲上科大生命科学与技术学院池天团队。(前排左1 陈玉鑫 前排左3 毛少帅 二排左5 荆征宇 二排左6 池天 二排左7 张校铭 三排 刘波)
昨天(7月22日),上海科技大学生命学院池天课题组在《细胞》(Cell)杂志在线发表论文,报道了一种崭新的小鼠基因打靶技术iMAP,快速鉴定了90个基因在39种组织的基本功能,构建了世界首张小鼠微型“扰动图谱”。
早在2001年,国际人类基因组计划就公布了人类基因组序列。但目前为止,约两万个哺乳动物蛋白编码基因在500多种细胞中的功能仍不为人知,这严重妨碍了疾病的诊断和治疗。
要系统性地解码全部基因在全部细胞中的功能,必须将其分别在各种细胞中敲除(扰动)再鉴定其细胞表型,即描绘完整的“扰动图谱”。
“扰动图谱”的完成,将成为生物医学研究的分水岭。此后,要探索任何基因的基本功能,将会像查找基因序列一样简单。但用传统的基因打靶方法,无法快速有效地描绘扰动图谱,成为功能基因组学领域久攻不下的瓶颈。
池天课题组里程碑式的成果为描绘完整扰动图谱迈出了从0到1的第一步。
iMAP融合了Cre-loxP和CRISPR-Cas9技术,其核心组成部分是一个转基因序列,它由U6启动子和下游一串gRNA表达单位构成。
转基因通常只表达第一个sgRNA,而利用药物(他莫昔芬)激活Cre,导致转基因重组,可使其余的sgRNA也得以表达,但每个细胞只随机表达其中一个。
这些sgRNA可在Cas9的帮助下敲除相应的靶基因,从而将小鼠转化为嵌合体。
这种嵌合体可立即用于描绘扰动图谱,也可迅速、廉价地繁育出多种传统的单基因敲除品系。该品系不但可用于特定靶基因的后续深入研究,更可用于个体水平的表型筛选,从而与嵌合体优势互补,共同加速基因解码。
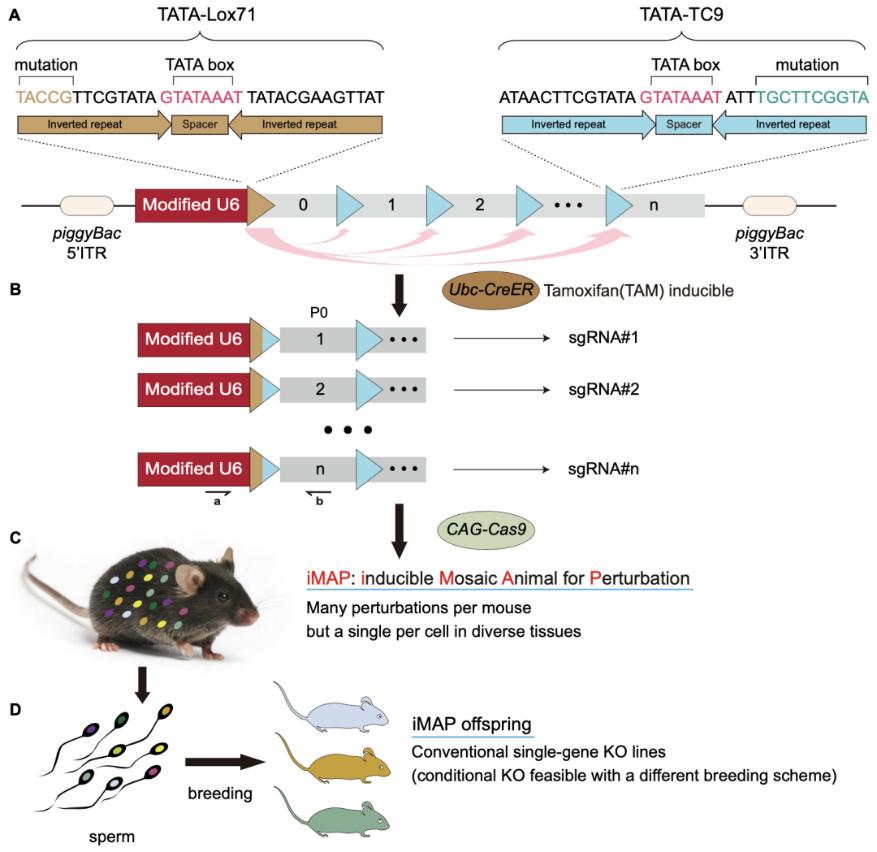
▲iMAP原理
iMAP诞生的背后是一场长达八年、历经六届学生前赴后继努力的科学“马拉松”。2014年,上海科技大学生命学院教授池天还在耶鲁大学,当时CRISPR基因编辑技术已问世,而池天又熟悉Cre-loxP。
他突发奇想,试图融合这两种技术,但同事并不看好。“有人不屑一顾,有人直呼疯狂,大多心存疑虑。”池天回忆,“这也不奇怪,因为iMAP太新了,是0到1,没有主流技术可以直接对标。就如同当年PCR概念萌芽后,甚至初步结果出来后,仍然在Cetus公司内部遭到冷遇,这好像不可思议,其实不难理解。”
iMAP的研发过程充满了艰辛和曲折。“我们踩了很多坑,有些坑很诡异。”为使同行避免重蹈覆辙,这些失败的实验,部分已于2年前以预印本形式发表。
经Ravinder Kaundal (耶鲁大学博士后)和陈玉鑫、毛少帅、刘波(分别是上科大生命学院2014、2015、2016级研究生)等的努力,到2018级博士生荆征宇加入课题组时,终于曙光初照,但道路依然坎坷。
除了学生非常给力,学校的大力支持也让池天的研究如鱼得水。
“我在耶鲁启动过其他数个像iMAP一样的高风险课题,但都因经费原因夭折了。而上科大鼓励教授勇于坐冷板凳,诺奖得主James Rothman也表示上科大适合我。所以我对学生说,课题必须做到底,论文非顶刊不发。”池天说。
据悉,研究团队构建了一个iMAP品系,它携带61个gRNA表达单位,共靶向6个功能已知的标志基因。该品系证明了iMAP的鲁棒性,包括展示转基因起码能稳定传13代。
随后构建的iMAP品系携带100个gRNA表达单位,靶向90个功能不甚清晰的基因,以此构建了一个微型扰动图谱,揭示了这90个基因分别在39个组织/细胞中对细胞存活、扩增、分化的影响。
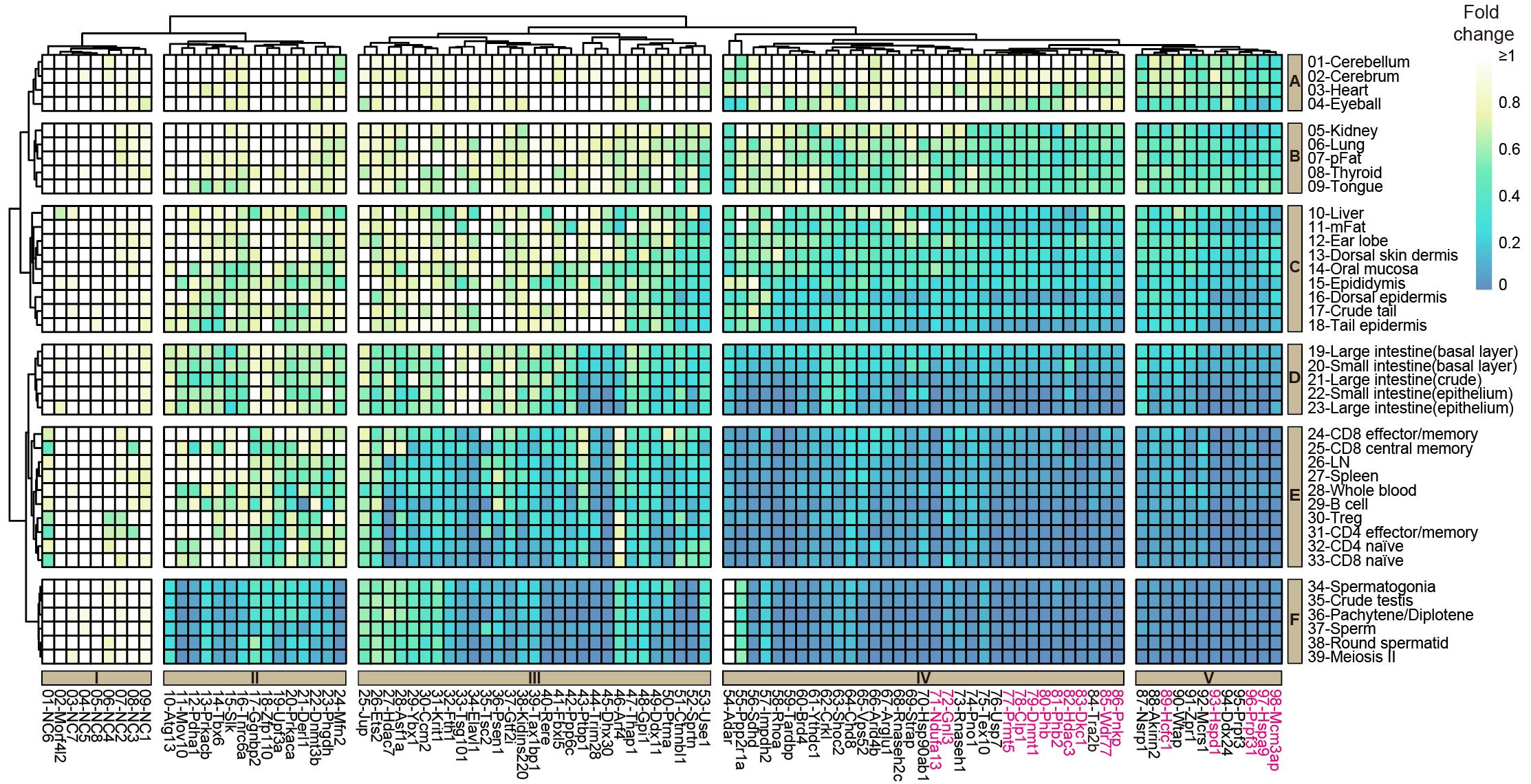
▲微型扰动图谱。展示100个sgRNA分别在39个组织/细胞类型中的丰度。
不但如此,研究团队还证明,一个iMAP品系的确可以衍生出多个传统的单基因敲除品系。
上海科技大学生命学院池天课题组2016级博士刘波(已毕业)、2018级博士生荆征宇、2019级博士生张校铭、2014级博士陈玉鑫(已毕业)、2015级博士毛少帅(已毕业)为本文共同第一作者,池天教授为唯一通讯作者。上海科技大学为第一完成单位。
作者:李晨琰
编辑:李晨琰
责任编辑:姜澎
*文汇独家稿件,转载请注明出处。





