
终于,肿瘤免疫治疗得奖了。今天傍晚,一年一度的诺贝尔奖开出今年的首个奖项,美国免疫学家詹姆斯·艾利森与日本科学家本庶佑因在肿瘤免疫负调节机制的发现,分享了2018年度的诺贝尔生理学或医学奖。
谈及获奖结果,多名科学家、医学家在与文汇报记者的交谈中用到一个词——“实至名归”。事实上,这两人及其所在的肿瘤免疫治疗领域此前就是诺奖大热门,两人被视作肿瘤免疫治疗领域的重要开拓者,其中詹姆斯·艾利森更被誉为“全球肿瘤免疫治疗的旗手”。值得一提的是,就在两年前,2016年的复旦中植科学奖正是颁给他们二人,这两人是不少中国科研人员的“老朋友”。
那么,他们两人研究的到底是什么?对肿瘤治疗的意义何在?记者多方采访获悉,两人长期从事的肿瘤免疫领域充满着荡气回肠的科学探险故事,其中有心酸,有挫折,更有着希望与曙光。他们的百折不饶,让肿瘤治疗取得突破进展。
肿瘤治疗重大突破:一个有关“松刹车”的故事
很多人说,如今已进入肿瘤免疫治疗时代。那么,肿瘤免疫治疗到底是什么?今年诺奖颁出的这个生理或医学奖到底在说什么?

人体有自身免疫系统,这不是一件新鲜事。简言之,当病毒、细菌等入侵人体时,人体会启动自身的免疫系统,抵御外敌。不过,当免疫系统失调时,就可能与上百种疾病的发生发展相关,其中就包括肿瘤。而今年的诺贝生理或医学奖说的其实是一个有关“松刹车”的故事。

▲2018年诺贝尔生理学或医学奖得主、美国科学家詹姆斯·艾利森
美国科学家詹姆斯·艾利森有两个重要的发现:第一是提出了免疫检查点的概念;第二,研发出了世界上第一种用于免疫肿瘤疗法的CTLA-4抗体。CTLA4被认为是免疫系统中一个至关重要的“刹车”,艾利森想到通过抗体阻断CTLA4功能,以增强一类T细胞对肿瘤的杀伤力。在动物实验中,他的方法被证明是可行的。

▲2018年诺贝尔生理学或医学奖得主、日本科学家本庶佑
日本科学家本庶佑的贡献是首次发现免疫检查点PD-1是激活T淋巴细胞的诱导基因,其后续研究进一步揭示了PD-1是免疫反应的负调节因子。形象地说,这是摸到了另一个“刹车”。
两人的发现均在上世纪90年代,此后沿着他们的研究方向,一系列重磅新药在本世纪相继诞生,由于临床效果显著,还被誉为“肿瘤神药”。
2016年的复旦中植科学奖正是颁发给了他们二人。“1994年,新的T细胞作用的机制不断被发现:原来我们以为通过这个信号的阻断,可以实现T细胞对癌细胞的攻击,后来发现其实这个信号本身是一个负面的信号,与其说给T细胞一个信号去攻击癌细胞,不如说我们通过对信号的阻断,可以解除对T细胞的限制,让T细胞对癌细胞展开必要的攻击。只要把这些信号关闭之后,我们的人体的这样的一个免疫系统,就可以持续地对癌细胞进行攻击。”詹姆斯·艾利森在复旦中植科学奖颁奖仪式上曾这样解释“松刹车”的概念。

▲通过“松刹车”来治疗肿瘤,图片来源:2018年诺贝尔生理学或医学奖官网
“对肿瘤的有效疗法既要踩油门,也要松刹车。”上海交通大学医学院附属仁济医院肿瘤科主任王理伟教授告诉记者,以往科学家对肿瘤的疗法倾向于“踩油门”,但获奖的两位科学家将目光瞄准“松刹车”,“两者相结合,T细胞杀死癌细胞的能力自然上升。”
这被认为是方向性的重要改变。“免疫是一个老概念,但免疫治疗应用于肿瘤治疗此前一直没有取得突破性进展,直到他们的原创发现,‘把刹车去掉’,让大家看到了曙光。”复旦大学附属华山医院外科主任钦伦秀教授说,这是一个厚积薄发的结果,全球此前投入了大量研究,肿瘤免疫治疗终于迎来突破进展。
临床成果显著,癌症患者盼来新生
从基础到临床,人们这次确实盼来了新机。
根据美国科学家詹姆斯·艾利森的研究结果,药厂研发制造了人源化CTLA4抗体,并对黑色素瘤治疗进行了临床试验,约有20%-30%的晚期病人有治疗反应。此后,美国药监局(FDA)很顺利地批准了这个药。
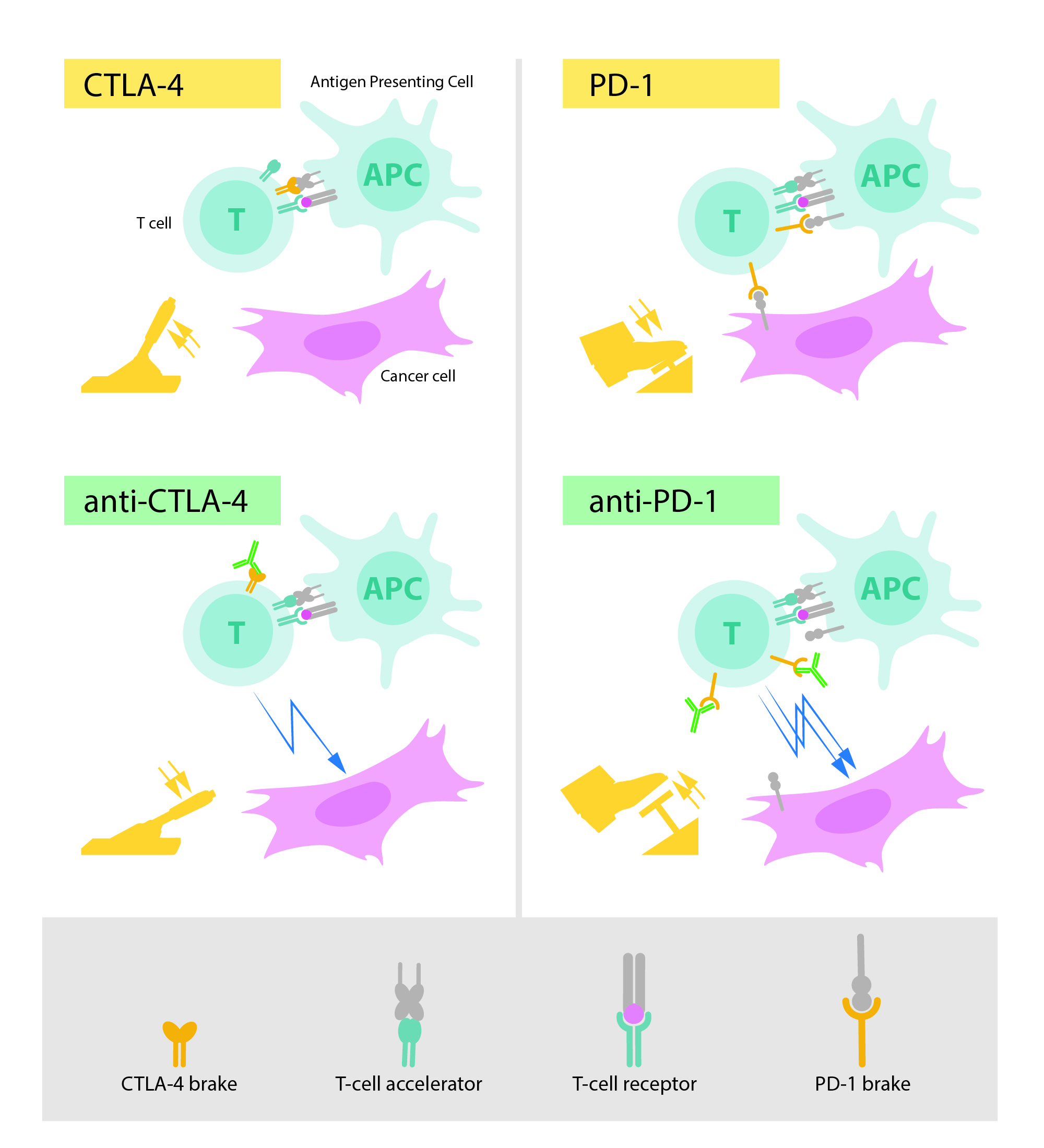
▲CTLA4和PD-1的工作原理(图片来源:2018年诺贝尔生理学或医学奖官网)
1998-1999年,日本的本庶佑课题组报道,PD-1在B和T淋巴细胞都表达,而且起到类似于CTLA4的负调节作用。由于CTLA4抗体的成功,多家公司也制造了PD-1抗体。其中,PD-1抗体对黑色素瘤的临床试验中首先获得突破,有比CTLA4抗体更好的治疗反应,已于2014年在日本和美国获得药监部门正式批准,对肺癌、淋巴癌、肾癌等多种肿瘤治疗都有不错的效果。另有报道称,CTLA4和PD-1抗体联用,在黑色素瘤治疗反应和多年存活率方面,均远远好于单一抗体。
“应该说,CTLA4、PD-1等科学发现帮我们进一步拓宽了对疾病认知的视野,进一步充实了我们的临床实践。”上海交通大学医学院附属瑞金医院肿瘤科张俊教授告诉记者,目前已有PD-1单抗和PD-L1单抗上市,PD-1单抗在黑色素瘤、微小细胞肺癌、结直肠肿瘤、胃癌等肿瘤中都有比较好的疗效。
上海市免疫学研究所研究员邓刘福告诉记者,免疫负调节的治疗效果临床上被广泛认可,尤其在治疗中国高发的癌症比如肺癌时效果较好。
说肿瘤免疫治疗成为全球实验室的“当红辣子鸡”并不过分。2013年,美国《科学》杂志把肿瘤免疫治疗推为当年最大科学突破之一。其中,有几个进展格外引人瞩目:继美国FDA2011年批准CTLA4抗体用于治疗黑色素瘤,PD-1抗体也在2014年获准用于同类肿瘤,并提前结束肺癌第三期临床试验。另外,CAR-T(嵌合抗原受体T细胞免疫疗法)技术在白血病治疗方面也有巨大成功。
可以说,无数患者盼来了新生。
痛彻心扉的支撑力,为向死而生的执着喝彩
不过,这个科学探险的故事并非一路都是艳阳高照的。
科研人员在与记者的交谈中均谈到,不论是詹姆斯·艾利森,还是本庶佑,两人的重要贡献还在于,全身心参与了免疫治疗在临床上的进行,让CTL4抗体、PD-1抗体等最终成为一种药物,成为患者可以用上的救命药。“而不像有的科学家在基础研究取得重要发现后,发表了大量论文,拿奖拿到手软就止步了。”
不过,医学临床转化的过程并不容易,甚至荆棘丛生。
以詹姆斯·艾利森为例,上世纪90年代,在加州大学伯克利分校的他发现抑制CTLA-4激活T细胞可以抑制黑色素肿瘤细胞的生长。为证明抑制CTLA-4是一个可行的肿瘤免疫疗法,他毅然离开伯克利来到斯隆凯特琳纪念(Memorial Sloan Kettering)癌症中心,担任路德维奇(Ludwig)免疫治疗中心的主任。就在那里,他与黑色素瘤临床专家Jedd D.Wolchok医生合作,共同开发Mederax(一家生物制药公司)研发的CTLA-4抗体,以治疗黑色素瘤。
艾利森曾回忆,当年CTLA-4抗体初上临床,找病人参加实验不容易。有位中年女性黑色素瘤患者在所有化疗手段失败后,依然有个顽强的念头:要活着参加孩子的高中毕业的典礼!多活几个月,就能熬到那一天。幸运的是,接受CTLA-4抗体治疗的她,不仅参加了孩子高中毕业典礼,还参加了孩子大学毕业典礼、婚礼等。不过,大多数病人没那么幸运。就像大多数新研发药一样,CTLA-4抗体也是几起几落,因为并不是每个病人都有效,这些病人还都是耐放疗化疗的晚期肿瘤病人,生存期大约只有半年。
相比CTLA-4抗体,PD1抗体的肿瘤疗效和应用层面要好很多,在黑色素瘤、肺癌、肾细胞癌均展现振奋人心的结果。不过,艾利森作为开路者的功劳实在功不可没。
“这是一项坚持了20多年的研究,这是一群执着的科学家,起初在人们还不是很理解肿瘤免疫治疗的时候,一度还有人说这是在死胡同里打转。”清华大学免疫学研究所祁海教授与文汇报记者谈及一个细节,詹姆斯·艾利森的很多家人死于肿瘤,艾利森的执着坚持、希望找到治疗肿瘤的办法,与这种痛彻心扉的支撑力不无关联。
原来,艾利森童年时母亲死于癌症,两个哥哥一个死于癌症,一个也患有肿瘤。他的一个叔叔也死于癌症。

▲年轻时的詹姆斯·艾利森
“也许正是因为家人有得癌的情况,让他对癌症的免疫治疗总显得那么投入,希望探索到用新的办法来治愈肿瘤。”复旦大学生命科学学院教授李继喜在2016年艾利森到访复旦领取中植奖时全程陪同了这名美国科学家,为他的幽默、执着、谦虚所感染。
有意思的是,艾利森走出实验室的业余生活是在一个小型乐队唱摇滚,别以为这乐队是随便进的,这个乐队成员全是肿瘤界大腕。而本庶佑也并非只有科学家的严肃一面。复旦大学药学院教授沈晓燕至今仍记得两年前初见本庶佑时的场景,“当时他戴着黑色的礼帽,穿着呢大衣,我还以为是大明星来了。”尽管只在上海停留了不到三天时间,但本庶佑的风趣、气质、风度却在沈晓燕心中留下了深刻印象,“他与我们印象中的科学家很不一样,很有生活情调,也很热爱运动。”沈晓燕告诉记者,“他跟我说,如果不做科学家的话,可能会成为一名高尔夫运动员。”
需要说明的是,免疫治疗并非肿瘤治疗的终点。受访专家均谈到,肿瘤治疗领域还有许多未解之谜,这群科学家的拓荒者贡献不可磨灭,新的发现会补充他们的发现,也可能彻底推翻他们的发现,因为还有很多问题没解决。比如,这类药物如何选择合适的人群,各类副作用如何克服,如何进一步提高疗效,如何与其他疗法的合作。
希望这群科学家能继续唱出肿瘤免疫治疗的新歌,希望终有一日,人类能免于与至亲好友过早道别的悲剧。
作者:唐闻佳 李晨琰
编辑:金婉霞
责任编辑:张鹏
*文汇独家稿件,转载请注明出处。





